Am un mare respect pentru acest statut VIIIA-grupuri.
Aceste elemente: heliu(El), neon(Ne), argon(Ar), cripton(Kr), xenon(Xe) (tse de bază), precum și radioactiv radon(Rn).
І formal, este posibil să se introducă bucată cu bucată otrimanie ununoktіy (Uuo).
Qia grup de elemente, de asemenea, voi numi propriul meu - aerogene, ale cel mai des sun nobil, abo gaz interior.
Inertnі Gazi
În același timp, activitatea de reacție este scăzută. Sub cuvântul „inerte”, există încă o lipsă de activitate. Nu știam prea multe despre asta de mult timp. Nu este posibil să te bazezi pe reacții suplimentare pentru ajutor. Viyavili їkh la povіtri (zvіdsi este numele aerogeni), după ce au văzut un pic de kissen și іnshi "gaze de mac", au scos azotul și l-au instalat experimental, astfel încât au scăpat de azotul din casă cu un asemenea rang. Privirile inerte s-au transformat în case de tsimi.
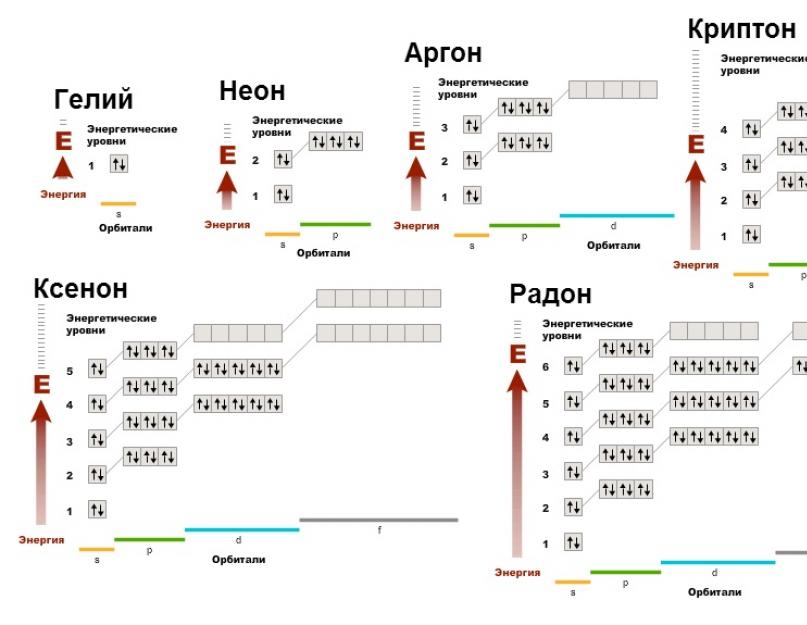
Inteligența, care este legată de activitatea de reacție scăzută a gazului, este necesară utilizarea acestor diagrame electronice:

Mi mogomo bachichi, scho fără electronice nepereche, orbital de stocare. Tse duzhe pryutkovy moara de înveliș electronic. Pentru asta și elementele din interior, stabilirea unei jumătăți de timp, pentru a ierta configurația electronică a ziarelor nobiliare (ghiciți regula octetului), unele dintre ele sunt vii din punct de vedere energetic, iar atomii, ca oamenii, trebuie să iubească într-un fel.
Prin inactivitatea atomului de gaze nobile, este imposibil să se acumuleze într-o moleculă diatomică (ca nucleu: O2, Cl2, N2 etc.).
Gazele nobile curg în jurul vederii moleculelor monoatomice.
A spune că gazul nobil este absolut inert este imposibil. Aerogenia Deyak poate fi în orbitali vilny la limitele unei ryvnya energetice, iar acest lucru înseamnă că există un proces foarte puternic de generare a electronicii. Nina, în mințile extreme superstițioase, a respins deyakis-ul „linivyh” spoluky din privirea activității chimice a elementelor. Ale in programe scolare, mai mult înăuntru, uită-te afară.
Puterea fizică
- heliu și neon s-au luminat spre bine, acele gaze nobile, care sunt mai mici - importante, care sunt mărite de creșterea masei atomice.
- prin receptorii de chimie, de savoare și miros, prezența gazelor nobile în mintea tuturor nu poate fi detectată, căci duhoarea nu miroase nici a savurare, nici a mirosului.
Semnificație practică gaze nobile.
Gel - tot felul de gaz pentru umplerea sacilor vechi, care este de a jefui vocea celor mai deștepți. Helium zapovnyuyut dirijabile (toate gazele, pe vidminu apă, nu vibukonesecure).
Gazele Shlyakhetnі și vikoristovuyut din tulpina atmosferei inerte (chimic inactiv). Deyak aerogeny intra în depozitul de sume dichal, kissen diluat (kissen este o oxidare puternică și dihotomie într-un viglyadi pur nu este posibilă).
Când este trecută printr-o descărcare de gaz nobil, duhoarea poate provoca puterea fluxului. Voi asigura un depozit de aerogen pentru echipamentele de iluminare. Viglyadaє pentru a termina specia.
Mai multe despre subiectul qiu:
- Puterea fizică.
- Autorități vesele.
- Istoricul afișării gazelor interne.
- Galuz zasosuvannya.
- Injecție asupra organizației oamenilor.
1. Puterea fizică a gazelor interne.
Gazele inerte nu provoacă culoare sau miros. І є monoatomic. Gazis inerți sunt nobilii vvazhayutsya. S-ar putea să văd conductivitate electrică (de regulă), iar când struma trece prin ele, se va aprinde.
Neonul este o lumină cu nume de vierme de foc, așa că cele mai frumoase linii se găsesc în zona roșie a spectrului.
Geliy - lumina yaskravoo-zhovtim, merită explicat că, în termeni de spectru simplu de sublinii zhovta linia perevazhaє peste usima іnshi.
Gazele inerte pot provoca cele mai joase puncte de creștere și îngheț, datorită prezenței gazelor din corpul molecular însuși. Se poate observa prin caracterizarea moleculelor atomice ale gazelor interioare.
2. Chimia puterii gazelor interne.
Gazul inert poate fi și mai puțin activ din punct de vedere chimic, ceea ce se explică prin configurația tare cu opt electronice a mingii electronice. Ca urmare a creșterii numărului de bile electronice, polarizarea atomilor în creștere. Otzhe, nu vei putea petrece o oră trecând de la heliu la radon.
Multă vreme în trecut nu cunoșteau mințile, pentru care oamenii nobili puteau să intre într-o relație chimică și să stabilească o conversație chimică corectă. Їхnya valență la zero. Primului grup nou de chimiști i sa dat un zero.
În 1924, a devenit evidentă ideea că unele dintre cele mai importante gaze energetice (zokrem, fluor și clorură de xenon) sunt stabile termodinamic și ar putea fi bazate pe minți pricepute. Teoretic, atât structura electronică a învelișurilor de cripton și xenon din pozițiile mecanicii cuantice, dar și gazul poate fi setat cu fluor.
Este o oră, dar în practică toate experimentele din întregul Galusi s-au încheiat cu eșec. Fluorura de xenon nu este activă. În continuare, am mers la visnovka, dar nu a fost păcat și până s-au obișnuit.
Abia în 1961, s-a născut în 1961 Bartlett, asociat al uneia dintre universitățile din Canada, în care s-a stabilit puterea hexafluorurii de platină, fără fluor în sine, având instalat potențialul de 12 în xenon inferior și fixând kissen cu hexafluorura de platină. la depozitul O2PtF6 ...
La temperatura camerei, Bartlett a furnizat hexafluorura de platină asemănătoare gazului și xenonul asemănător gazului, eliminând o vorbire solidă galben-portocalie, pe care a numit-o XePtF6 hexafluorplatinat la xenon.
Când este încălzit în vid, hexafluoroplatinatul XePtF6 trebuie încălzit fără pliere. Alunecă pe lângă apă, vezi xenon:
2XePtF6 + 6H2O = 2Xe + O2 + 2PtO2 + 12HF
Înainte ca Bartlett să rostească un nou discurs, Bartlett s-a dus la muncă, dar comportamentul hexafluorplatinatului nu trebuie văzut din comportamentul chimiștilor răi.
Roboții lui Bartlett au lăsat să stea, dar xenonul a fost depus în mintea reacției, construind uși cu hexafluorură de platină: XePtF6 și Xe (PtF6) 2. Dacă există o lipsă de hidroliză, există doar unul dintre cele mai bune produse.
1962 pentru a rock Bartlett se împiedică pe fundal.
Deja trei ani mai târziu, experimentul a fost repetat de un grup de prelați americani în Laboratorul Național Argonne de la Choly cu Cernik. Să luăm în considerare pentru prima dată la distanță sinteza spoluk-urilor analoge xenonului cu hexafluoruri de ruteniu, ruteniu și plutoniu.
Acum, în primul rând, xenon: XePtF6, Xe (PtF6) 2, XeRuF6, XeRhF6, XePuF6
Mitul despre inerția absolută a gazelor nu este confirmat.
Există o ipoteză despre posibilitatea interacțiunii directe între xenon și fluor.
Am pus mult gaz (1 parte xenon și 5 părți fluor) într-un vas de nichel, ca cea mai bună soluție pentru fluor, și l-am încălzit cu o menghină mică.
Pe parcursul unui an, nava a fost răcită, iar gazul a fost pompat. Gazul, care se revărsa, nu a apărut, ca fluorul. Tot xenonul a reactionat!
Apoi, la vasele deschise, ei vyavili fără cristale de hambar la tetrafluorura de xenon XeF4.
Într-un lanț de soluții, molecula are forma unui pătrat cu ioni de fluor de-a lungul tăieturii și xenon în apropierea centrului.
Tetrafluorură de xenon XeF4 fluor mercur, platină (diluat cu fluorură apoasă): XeF4 + 2Hg = Xe + 2HgF2
În mod miraculos, cei care modifică reacțiile pot fi respinși ca XeF4, și aceeași fluorură, de exemplu XeF2, XeF6.
V.M. Khutoretskiy și V.A.
Ele sunt folosite pentru a propune o modalitate, dacă cantitatea de xenon și fluor (la un raport molecular de 1: 1) este introdusă într-un vas dintr-un pahar de oțel inoxidabil, iar când presiunea este împinsă până la 35 atm, reacția este reparat.
XeF2 - Fluorură de xenon unic, cu o descărcare electrică injectată de xenon și tetrafluorură în carbon, fără fluor.
XeF2 pur este eliberat atunci când xenonul și fluorul sunt optimizate de ultraviolete.
Difluorura XeF2 are un ușor miros specific.
Rezistența la difluoruri în apă este scăzută. Yogo roschin este cel mai puternic agent oxidant. Probabil cu auto-glațarea pe xenon, kisen și apă cu fluor. In mijlocul piscinei, distributia este deosebit de rapida.
p align = "justify"> Metoda pentru sinteza difluorurii de xenon, bazată pe injectarea în suma gazelor de viprominuvannya ultraviolete (până la 2500-3500 A) este de mare interes teoretic.
Viprominuvannya wiklicaє scindarea moleculelor de fluor în atomi vilny. Primul motiv pentru aprobarea difluorului, deoarece fluorul atomic este activ supraspecific.
Pentru a respinge hexafluorura de xenon XeF6, este necesară cantitatea necesară de energie: 700 ° C și 200 atm. Pentru astfel de minți, suma xenonului și fluorului, de la 1: 4 la 1: 20, practic tot xenonul va fi convertit în XeF6.
Hexafluorura de xenon este superficial activă și se pliază cu vibuch.
Reacționează ușor cu fluorurile metalelor străine (crim LiF): XeF6 + RbF = RbXeF7
Chiar și la 50 ° C, sil se prăbușește: 2RbXeF7 = XeF6 + Rb2XeF8
Fluorura vâscoasă XeF8 este stabilă la temperaturi sub minus 196 ° C.
Chiar și mai devreme, gazele nobile au fost văzute în vecinătatea grupului nul, dar a fost complet informat despre valență, apoi sinteza primei jumătăți de xenon a fost pusă în fața chimiștilor sursei de alimentare pe la mijlocul interiorului. sisteme de gaze. Gazele inerte au fost decise să se transfere în grupa a VIII-a, dacă au devenit o specie cu cea mai mare fluor, valența xenonului este mai mare de opt, așa că poate fi folosit complet din mugurul carcasei electronice.
Eliminați fără efort fluorurile din xenon. Xenonul Zmushiti intră într-o reacție fără participarea fluorului (unele dintre ele spoluch) fără a ajunge nicăieri.
Vă rugăm să vivcheno schimbul de fluoruri de xenon cu apă.
Când XeF4 este hidrolizat într-un mediu acru, se formează oxidul de xenon XeO3 - cristale fără bare, care pot fi topite.
Molecula XeO3 are structura unei piramide triunghiulare stropitoare cu un atom de xenon în vârf.
Tse duzhe nestіyke z'єdnannya, atunci când este desfășurat, îndemnul vibuch-ului de a se apropia de îndemnul vibuch-ului TNT. Pentru asta, câteva sute de miligrame de XeO3 sunt suficiente, exxicatorul a fost zdrobit în bucăți.
În perspectiva transferului vicarystannya la trioxid de xenon iac vibukhivka. O astfel de vibuchivka a unui glonț ar fi mai manuală, astfel încât toate produsele unei reacții vibuchiv sunt gaze. Este scump ca trioxizii de metil xenon să scape de ei din cauza rezervelor mici din atmosferă și a plierii tehnice.
Pentru a elimina 1 m3 de xenon, este necesar să spargeți 11 milioane m3 de răsucire.
Acidul nerezistent al xenonului hexavalent H6XeO6, care este similar cu trioxidul, se stabilește ca urmare a hidrolizei XeF6 la temperaturi de 0 ° C:
XeF6 + 6H2О = 6HF + H6XeO6
Chiar înainte de produsele lanțului de reacții, este necesar să se adauge Va (OH) 2, vipada biliu amorf
asediu Ва3ХеО6. La 125 ° C, vinul se depune pe oxid, xenon și oxigen.
Saruri analoge Otrimano-xenonat de sodiu si calciu.
De la ozon până la gama de XeO3 în hidroxid de sodiu un-molar, acesta este configurat cu acidul acid și xenonul Na4XeO6. Perxenonatul de sodiu poate fi văzut sub forma unui hidrat cristalin fără bare Na4XeO6 · 6H2O. De asemenea, până când perxenonații sunt aprobați, induceți hidroliza XeF6 în hidroxizi de sodiu și calciu.
Este suficient să măcinați Na4XeO6 solid cu o soluție de nitrat de plumb sau chiar uraniu și unii dintre următorii perxenonați:
Ag4XeO6 este negru, bXeO6 și (UO2) 2XeO6 este negru.
Sărurile analoge dau calciu, calciu, litiu, cesiu.
Iac în octafluorura, valența la xenon este de până la opt.
Chotirikis solid la o temperatură de 0 ° C se descompune în xenon și muselină și asemănător gazului (la temperatura camerei) - în trioxid de xenon, xenon și mussen.
Molecula XeO4 are forma unui tetraedru cu un atom de xenon în centru. Există două moduri de a trece de la hidroliză la hexafluorura de xenon:
- introduceți tetraoxifluorura XeOF4,
- introduce dioxifluorura XeO2F2.
Sinteza directă a elementelor pentru a produce oxifluorura XeOF2.
Recent a fost injectat în reacția difluorurii de xenon cu НС1O4 anhidru.
Otrimano nou la xenon XeClO4 este un agent oxidant obositor, ca urmare a întregii reacții este cel mai puternic perclorat. Sintetizat cu jumatate de xenon, pentru a nu se razbuna pe acru.
Lanțul de sub-săruri, produse ale interacțiunii fluorurilor din xenon cu fluorurile de surmi, mish'yak, bor, tantal: XeF2 · SbF5, XeF6 · AsF3, XeF6 · BF3 și XeF2 · 2ТаF5.
Am vorbire nareshty, confuză tip XeSbF6, stil pentru temperatura camerei și XeSiF6 este un complex instabil. În această zi, ridică-te în depărtare, acel radon interacționează și cu fluorul, făcând fluorul nevolatil.
Am văzut diferența dintre difluorura KrF2 și tetrafluorura pentru kriptonul KrF4 dincolo de puterea care poate fi utilizată pentru jumătate din cantitatea de xenon. 4. Istoricul afișajului gazelor interne. Înainte de gazele nobiliare se află heliul, neonul, argonul, kriptonul, xenonul și radonul. Pentru puterea sa, mirosurile nu sunt asemănătoare cu cele ale elementelor, iar în sistemul periodic ele cresc între metale tipice și nemetale.
Istoria dezvoltării gazelor energetice este de mare interes: în primul rând, ca un triumf introdus de Lomonosov unor metode de chimie (în cazul argonului), și cu alte cuvinte, ca un triumf al transmiterii teoretice.
Inspecția de către fizicianul Releu și chimist Ramzam a primului gaz nobil - argonul - a fost introdusă la acea oră, dacă sistemul periodic era finalizat și câteva celule goale erau lipsite de ele.
Încă din 1785, chimistul și fizicianul englez G. Kavendish a găsit la începutul zilei noi gaze, o chimie superb de stabilă. Aproximativ o sută douăzeci de părți din obsyagu povitrya au căzut în fața gazului. Ale scho tse pentru gaz, Kavendish z'yasuvati nu a ajuns.
Aproximativ 107 soarta s-a ghicit despre asta, de când John William Stratt (Lord Rayleigh) l-a frecat pe aceeași casă, ținând cont că azotul este mai important, mai puțin azot, viziuni din spoluk. Neștiind o explicație sigură a anomaliei, Rayleigh, prin jurnalul „Nature”, s-a adresat colegilor-naturaliști și a sugerat imediat să se gândească la asta și să încerce să rezolve problema motivelor.
După două rachete, Raleigh și U. Ramzai s-au ridicat, în azot, este o casă de gaz nemaiauzit, important pentru azot, și la limita chimiei inerte.
Bine, pentru niște muzică de copt în plus, adăugați puțină aciditate și apoi încălzește puțin magneziu într-un tub cu câteva bucăți mici. În plus, deoarece cantitatea de azot este semnificativă, bolul este blocat cu magneți, cantitatea de azot este determinată de cantitatea de surplus.
Rentabilitatea a fost de 15 ori mai mare pentru abundența apei, în timp ce abundența azotului a fost de doar 14 ori mai mare pe an. Nivelul de competență a crescut și a preluat utilizarea azotului, docurile au ajuns la 18.
Așa că s-a spus că gazul este mai probabil să fie răzbunat, al cărui procent este mai mare pentru azot... Wono vyavilsya gaz monoatomic.
Dacă duhoarea a venit de la știrile publice despre atac, atunci ostilitatea a fost făcută într-un mod viclean. Bagaty arăta ca un neymovyr, dar încă câțiva discipoli, ca o mie de analize, s-au uitat unul la altul. parte de depozit, același taku își va aminti - mayzhe vidsotok! Până la discursul, în aceeași zi și în aceeași an, 13 secera în 1894, argonul și-a tăiat imaginea, care în nuc înseamnă „nu mare”.
Heliu înainte de identificare element chimic iac la 1868 p. P. Zhansen în timpul dezvoltării întunecării somnolenței în India. În timpul analizei spectrale a cromosferei somnoroase, a fost dezvăluită o linie, care a fost adusă la spectrul sodiului, dar în 1871 J. Lok'єr și E. Frankland au numit noul element heliu vid nuci. „Helios”, care înseamnă soare.
Todi nu știa dacă heliul era un gaz inert, dar i-au dat drumul, dar era metal. Și numai după un sfert de secol de apariție a heliului pe pământ. În 1895, după câteva minute de scris către argon, U. Ramzai și imediat chimiștii suedezi P. Cleve și N. Lengle s-au ridicat, că gelul a fost văzut când mineralul a fost încălzit.
Prin Rik G. Keyser, a dezvoltat o casă cu heliu în atmosferă, iar în 1906 a înflorit cu heliu la o instalație de stocare a gazelor naturale din adâncurile naftei din Kansas. În același timp, au fost instalate E. Rutherford și T. Royds, care a-părți, care sunt eliberate de elementele radioactive, є un nucleu de heliu.
Pentru întregul afișaj va funcționa Ramzai, care este un întreg grup de elemente chimice, care în sistemele periodice sunt amestecate cu metale și halogeni. Corodat de legea periodică și de metoda lui Mendelev, o serie de ziare și puteri neimplicate, un vlăstar de mași atomic a fost desemnat. Tse a permis fanilor să obțină glumele ziarelor nobili.
Ramzay și sportivii yogo erau ocupați cu minerale, ape naturale și meteoriți la zgomotul gazelor interioare. În semn de protest, totul a explodat în zadar, analizele s-au dovedit invariabil negative.
Tim are o oră - au un gaz nou, dar nu au folosit metodele, nu le-au folosit pe cele sensibile și nu le-au folosit.
După ce ați auzit până la sfârșitul zilei, toate pentru următoarele momente ale rock-ului care urmează, veți vedea noile elemente, precum și gaze, precum neonul, kriptonul și xenonul, veți vedea viziunile de la început.
Pentru o grămadă întreagă, curățat în fața dioxidului de carbon și în teologie, zridzhuvali, și apoi reparat viparovati. Pe parcursul întregii proceduri, nu ar trebui să ai suficient gaz pentru a vaporiza și energie importantă, dar ai pierdut cantitatea de vaporizare și o folosești.
Fracțiunile otrimanizate au fost date tinerilor.
Analiza spectrală este ușor de înțeles, fiind una dintre metodele utilizate pentru determinarea valorii:
Este o procedură simplă care permite identificarea gazului fără energie de-a lungul liniilor intervalului.
Pentru întregul gaz, acesta se pune în tubul de distribuție, înainte de conectarea conductei.
Dacă pun prima, cea mai bună și fracțiunea cu fierbere scăzută în tub, atunci în spectrul ordinului cu liniile vizibile de azot, heliu și argon, apar linii noi, în special gloanțele strălucitoare ale viermilor. Duhoarea revărsa lumină în țevile din focurile hambarului. Istoricul Cіkava nume gaz:
Dacă Ramzai sposterіgav, lângă Chergovyu dosvіdі, spectrul gazului bine tăiat, înainte de laboratorul uvіyshov yogo dvadtsyatirichny păcat, care a primit statutul de "shanuvalnom" roboții tatălui... După ce ați reparat iubita nevicioasă, câștigați viguknuv: "unul nou!" , scho greaca veche înseamnă „nou”.
Așa că Vinikla a numit gazul „neon”.
Să cunoască gazele interioare, cum să completezi sferturile, noțiunile și primele perioade ale tabelelor mendeliane, în depărtare nu deodată, fie doar din cauza flăcării de heliu, neon și argon, cum să parcurg primele trei etape a tabelului mendelian, în primul rând
Ale, la acea oră, au venit cu puțină mâncare savuroasă, mult zavdyak la eforturile tânărului englez Traverse.
Devenind accesibilă apei native.
I Ramzai imediat de la Traverse a putut să se ocupe de ultimele evenimente importante ale zilei, cum să merg să trimită mesaje către heliu, apă, neon, acid, azot și argon.
Zalishok otrimav Siria (nepurificare) krypton. Prima dată când l-am văzut în vas, am primit mult gaz. Toate gazele oferă o gamă largă de linii în zonele de la portocaliu la violet și lumina mav blakitne în priza electrică. De fapt, liniile spectrale pot fi folosite pentru a identifica un element fără fast. І Ramzai și Traverse mali sunt toți furnizați cu o nouă sursă de gaz.
Îl voi numi xenon, care în nuc înseamnă „extraterestru”. Chiar dacă facțiunea Krypton este o străină, este adevărat.
La glumele unui nou element al vivchennya autorităților, Ramzai și Travers au zdrobit aproape o sută de tone de hrană crudă. Zm_st la xenon în atmosferă nu este suficient, dar chiar mai mult - practic nu este plictisitor la xenon (ar putea transforma tot xenonul în atmosferă).
A fost instalată individualitatea xenonului ca element chimic nou, care operează mai puțin de 0,2 cm3 de gaz.
Ramsay poate să-și asume creditul pentru mesaj înalt reprezentant gaze inerte. Vikoristovuchi fine tehnice priyomi, vin doviv, astfel încât radioactiv se întoarce de la radio - emanație radio - este un gaz care este în conformitate cu toate legile gazelor moderne, un spectru inert chimic și caracteristic scăzut. Ramzai vimіryаv fluiditatea difuziei, care a permis stabilirea greutății moleculare a gazului, scho să devină aproximativ 220:
Când nucleul atomului emană de la radio - întregul surplus al nucleului este trimis către heliu (particule a -), atunci sarcina atomului este responsabilă pentru 88-2 = 86. Astfel, noul element buty cu gaz inert. O mașină atomică yogo 226-4 = 222. Oficial, a fost încălcat includerea unui nou grup de elemente chimice în sistemul periodic la 16 martie 1900, cu ajutorul lui Ramzai din Mendelev.
- Zona de stocare a gazelor interne.
Geliy - dzherelo de temperaturi scăzute.
Ridkiy heliu vikoristovutsya urăsc adesea ovarele, de exemplu, supraprovodnіst într-o stanі fermă. Epuizarea termică a atomilor și electronilor electrici din corpurile solide este practic în afara zilei la temperaturi scăzute de heliu.
În plus, heliul rar este excelent pentru răcirea supraveghetorilor magnetici, stropirea particulelor și a anexelor. Livrați la aspirație neinvizibilă heliu ca agent de răcire, є procesul de reducere neîntreruptă a 3He și 4He, pentru setarea și reglarea temperaturilor mai mici de 0,005 K
Heliu asemănător gazului vikoristovuyat yak gaz ușor similar cu sacii uscati.
Oskil a câștigat neinflamabil, її її її її її її її її її її її la zapovnenya pentru carapacea aeronavei, terminând până la apă.
Heliu vikoristovuyak ca mijloc interior pentru încălzirea arcului, în special magneziu și acel aliaj, atunci când sunt eliminate Si, Ge, Ti și Zr, pentru răcirea reactoarelor nucleare.
Інші stocarea heliului - pentru masticarea gazelor lagărelor, pentru detectoare de neutroni (heliu-3), termometre cu gaz, spectroscopie cu raze X, pentru transmisii de gaze, pentru pompe izvoare înalte... În vârful celorlalte gaze nobile, heliul este vicios la ultimele reclame cu neon (la tuburile cu descărcare în gaz).
Există o mulțime de stază de heliu în mintea nebunilor pentru robustețe, adică heliul este mai bun în sânge, mai puțin azot. De exemplu, cu foraje de mare, cu deschideri subacvatice tuneluri și sporud.
În cazul heliului vikoristanny, viziunea de gaz epuizat din sânge, decompresie, scafandru are o mulțime de dureri, există puțină boală la scafandru.
Ezitantul He – O2 stagnează vâscozitățile scăzute pentru persoanele cu crize de astm și pentru copiii vechilor boli bolnave.
Argonul este utilizat pe scară largă pentru depozitare.
Durabil zruchno arc electric de încălzire în mijlocul de argon, tk. într-un jet de argon, puteți arde subtilitățile virobiului și ale metalului, care erau importante mai devreme. Vvazhaєtsya, cum un arc electric într-o atmosferă de argon a adus o revoluție în tehnologia producției de metal. Procesul s-a accelerat rapid, a existat posibilitatea de a tăia foile de metale refractare.
Când argonul este suflat prin oțel, acesta poate vedea gazele incluse. Voi reduce puterea metalului. Arcul de argon este suflat prin argon (în cazul apei), marginile sunt înfășurate și electrozii de wolfram sunt fabricați din oxid, nitrură și alte margele. O oră, șterg mânerul și concentrez arcul pe o suprafață mică, după ce temperatura din zonă ajunge la 4000-6000 ° C.
În plus, fluxul de gaz este un fel de dezvoltare a produsului.
Și atunci când este ars într-un jet de argon, nu este necesar să se utilizeze fluxuri și electrozi și apoi, la curățarea cusăturii de zgură și surplus de flux.
Zastosuvannya xenon, adesea runtutsya pe sol pentru a intra într-o reacție cu fluor.
În cazurile medicale, xenonul s-a extins cu fluoroscopia în creier. Stagnați cu iluminarea intestinală (xenonul se agață puternic de xenon viprominuvannya și ajutor suplimentar pentru a cunoaște problema). În același timp, nu este deloc timid.
Și xenonul izotop activ, xenon - 133, vikoristovuyut la eficiența funcțională avansată a inimii.
Tehnologia luminii are o gamă largă de lămpi cu xenon și o menghină înaltă. Principiul de a face acest lucru este de a fi ghidat de faptul că în astfel de lămpi se produce o descărcare cu arc în apropierea xenonului și că există o prindere de zeci de atmosfere.
Lumina din astfel de lămpi este strălucitoare și fără întrerupere spectrul - de la ultraviolet până la regiunea infraroșu apropiat și apare imediat ce este pornită.
6. Diya despre organizarea oamenilor.
Va fi firesc să respecte, dar gazele nobile nu se fac vinovate de revărsare asupra organismelor vii, ceea ce este foarte mișto. Totuși, nu este așa. În nebunia acrișiunii, inhalarea altor gaze energetice este de a aduce oamenii în tabără, până la spiritele alcoolice. O astfel de acțiune narcotică a gazelor interioare se acumulează în diferențele dintre țesuturile nervoase. Primul lucru este că este un gaz inert de energie nucleară, că este mai eficient și că este mai narcotic pentru că este o presiune mare.
Lista literaturii.
- Guzei L.S. Prelegeri de la chimie acasă
- Akhmetov N.S. „Zagalna și chimia neorganică”
- Petrov M.M., Mikhil'ev L.A., Kukushkin Yu.M. "Chimie anorganică"
- B.V. Nekrasov „Chimie Pidruchnik zagalnoy”
- Glinka N.L. „Zagalna Khimiya”
La zvaryuvanni este adesea numit vikoryuvannі așa-numitul gaz іnertnі. Înaintea lor, există un grup de elemente chimice, care pot avea caracteristici similare. Gazul inert este nobil pentru mințile normale є monoatomic. Practic, toate mirosurile nu miros nici culoare, nici miros. Reactivitatea caracteristică este și mai mică în chimie. Mirosul este practic pentru a nu intra într-o reacție cu metalele, ceea ce este necesar pentru un robot normal. Astfel de gaze ocupă primele 6 perioade și se referă la al optulea grup de elemente chimice din tabelul periodic.
Puterea gazelor interioare poate fi explicată din teoria structurilor atomice. Mirosul iese din învelișurile electronice de la electronii de valență. Gândiți-vă doar, în care discursurile pot lua o soartă lipsită de un număr mic de reacții chimice. Desigur, pentru toate gazele nobile mai mici de 10 grade pe Celsius, este practic ca toate gazele nobile să țină cont de temperaturile de fierbere și de topire.
Galuz zasosuvannya
Puterea gazelor interioare de a le opri și mai mult solicitată din sfera sănătății. Principalele metode de depozitare sunt arderea cu gaz și cu arc de gaz. Miros vikonuyut rolul de mijloc zhisny, ca o baie vidgorodzhuv cu metal de topire de la afluxul negativ al altor factori, inclusiv mijlocul alimentar. De regulă, duhoarea stagnează în același timp cu acru tehnic, iar așchiile vor crește temperatura cuptorului. În cazul gazelor interioare victorioase, acestea merg din ce în ce mai mult și din nou, dar suma de bani scade ore în șir.
Rechivini vikoristovuyutsya pe maidanchiks minunat cu instalarea de structuri metalice, în special părți neporoase. Sunt proiectate eficient cu detalii delicate, tevi si alte obiecte, care pot fi adaptate usor la sunetul electric. În atelierele de reparații pentru actualizarea mașinilor și a tehnologiei de pliere, nu este suficient să folosiți gaze inerte ca metodă principală de îndepărtare a pieselor și există puțină pierdere de timp cu materialul. În sfera comunală, este necesar să vorbim despre repararea țevilor și alte discursuri și, de asemenea, trebuie să vorbească despre asta. Când virobnitvі metal virobіv de tip roz, în special din metale colorate, este ușor de aprins, gazul inert este nobil în siruvina principală pentru roboți.
Perevagi
După ce a crescut, înseamnă gaz inert, varto zrozumiti, care este în sine atât de popular cu tsiy galuzy. Tse este turnat alături de un număr de perevag, yaki runtuyutsya pe puterea yogo. Desigur, pot avea propriile lor specialități, dar, în general, puteți vedea astfel de momente pozitive:
- Rechovina practic nu intră într-o reacție cu metalele, care sunt efectuate de un robot, suntem acri, suntem prea slabi;
- Gazul este lăsat să atingă temperatura ridicată în timpul gătirii, ceea ce va împiedica gătirea pentru o cantitate mai mare de metal;
- Є Posibilitatea de a regla jumătatea minții, yogh spivvidnoshennya cu acru pentru respingerea autorităților necesare;
- Zberigannya și transportat din tabăra de adulți, sau sub o strângere mare, să apară cu un mare drept pentru compactitate;
- O vedere a acestor gaze poate fi instalata fara a fi nevoie de a priori pe statia de lucru pentru instalatiile speciale ale generatoarelor.
Incomplet
Tim nu este omul, vreau pentru o mulțime de galuzy gazi și una dintre cele mai comune soluții, їkh vikorstannya mici deficiențe, ale căror mijloc sunt principalele:
- Zberigannya și baloane transportate din gaze є pentru a termina cu un drept de pliere, resturi є risik vibuhu;
- Cele mai multe dintre cuvintele de acest fel se îndreaptă spre otravă, dacă concentrarea lor în ziua următoare atinge valoarea cântării;
- Deyakі gazi este douzhe shkіdlivі pentru organele de educație și mozhut viclikati afectiuni profesionale pentru o perioadă relativ scurtă de timp este necesară o oră pentru asta PERSOANE FIZICE zahist;
- Acetilena și alte gaze pot fi o mulțime de muncă, astfel încât procesul de gătit este mai costisitor.
Vedeți gazele interioare
Argonul nu este de marcă, nu miroase a culoare. Câștigul este important pentru creșterea dimensiunii de 1,5 ori. Gazul nu iese în metale, cum ar fi în solid sau în oțel dur. Pentru promislovostі vypuskayut la viglyadі primului soi. Varietatea Vyshy răzbună 99,993% din vorbirea pură și devine stagnantă în cazul sporilor în creștere. Prima clasă dezvăluie 99,98% vorbire pură. Aditivi pentru iac є azot și gâscă. Bine de plecat.

Geliy nu este otruyny, nu miroase ca acea culoare. Câștig pentru noroc. Rechovina este autorizată să respecte GOST 20461-75. Poate exista gaz tehnic cu o puritate de 99,8% și un grad de puritate ridicată de 99,985%. În zvaryuvanny vikoristovuyutsya nu atât de des, ca argon, atât de drag și deficitar. Win poate fi mai eficient, deoarece arcul a văzut cu ei mai multă energie și mai puține daune și mai multă fierbere. Principala sferă de victorie este prepararea de materiale active și pure din punct de vedere chimic pe bază de magneziu și aluminiu.

Azotul nu este de marcă, nu miroase a culoare. Freeze pentru dezvoltarea muzicii și aliaje pentru metal. Este emis în conformitate cu GOST 9293-74 și standardul include 4 soiuri principale. Whisky-ul are 99,9% material pur, primul are 99,5%, celălalt are 99%, iar al treilea are 97%.
![]()
Instrucțiuni pentru supt
Când vikorystannі іnertnyh gazіv miros în Persha, porniți într-un palet, pentru a-și reconsidera prasezdatnіst. Puteți adăuga kissen numai la mâncare. Jumătate din aceasta poate fi victorioasă pentru jocul frontal și realizarea pas cu pas, și nu doar pentru logodnă. Pe cob, este necesar să se afișeze parametrii de alimentare cu gaz și să se alimenteze în modul necesar.
Înainte de a începe cob, este necesar să schimbați toate furtunurile pentru o funcționare corectă, astfel încât gazul să nu provină din ele. "
Intră în siguranță
- Baloni cu gaz sunt cunoscute a fi la locul de 5 metri de jumătatea dzherela și discurs ușor împrumutat;
- Aproape nu este de vină pentru plajele uleioase;
- Timp de o oră, robotul baloni poate fi fixat în siguranță;
- Este necesar să aveți grijă de tabăra de poluare cu gaze, astfel încât să nu existe miros de aer.
Zberigannya și transport
Transportul se face vinovat de a fi efectuat pe transport cu rezoare. Baloni sunt vinovați, dar sunt reparați, dar nu îi pot dezamăgi, lovesc pe unul și cad. Zberigannya este vinovat că a fost efectuat în mediul rural, astfel încât să vă puteți testa.
Visnovok
Neimportante pentru toate deficiențele și pliabilitatea, gazele inerte sunt copleșite de materialele vitratice solicitate pentru un sunet bun și de înaltă calitate.
Școala Internațională Britanică
Rezumat din chimie
„Ziare și autorități inerte”
Scoala a 9-a clasa b
Sokolenko Oleksiya
Kerivnik:
Cernishova I.V.
I Intrare ………………………………………………………………………………… 2
1.1 Іnertni gazi - elemente ale grupului VIIIA …………………………………… ... 2
1.2 Argon de pământ la allsvit ………………………………………………… .5
II Istoricul detectării gazelor ……………………………………………………… .................. 7
2.1 Argon ………………………………………………………………………………… 7
2.2 Geliy …………………………… .. ……………………………………………………… ..8
2.3 Krypton ……………………………………………………… .. ………………… ..9
2.4 Neon ……………………………………………………… .. ………………… 9
2.5 Xenon …………………………………………………………………….. ……………. …………… .9
2.6 Radon ………………………………………………………… .. …………… .10
III Puterea gazelor inerte și spoluk …………………………………………………………………………………………………………… ..... 10
3.1 Puterea fizică a gazelor interne ………………………………………… .10
3.2 Chimia puterii gazelor inerte ………………………………………………………………………………………………………………………… …… ..... 11
3.3 Respingerea argonului …………………………………………… ... ………… ..14
3.4 Autoritățile fiziologice ale gazelor interne ……………………………………………… 15
IV Stagnarea gazelor inerte ……………………………………………… ..… ..16
Lista literaturii victorioase …………………………………………… .... 18
eu
Skryz și peste tot voi părăsi atmosfera bunătății. De la cine e? Răspunsul este incomod: de la 78,08 la azot, 20,9 la oxigen, 0,03 la dioxid de carbon, 0,00005 la apă, aproape de 0,94 la o fracțiune din așa-numitul gaz interior. Restul mingilor au cunoscut pierderea secolului trecut.
Radonul se stabilește în cazul unei scăderi radioactive a radioactivității și în orice cantitate de material, care dezvăluie uraniu, precum și în unele ape naturale. Heliul este un produs al dezintegrarii α radioactive a elementelor, care se găsește uneori în gazele naturale și gazele, care pot fi văzute din găurile de naftă. Numerele maiestuoase ale cei au un element care să aibă loc pe Cântecele și Stelele. Există un cu totul alt element de lățime în orice moment (deocamdată).
1.1 Gaz inert - elemente din grupa 8A.
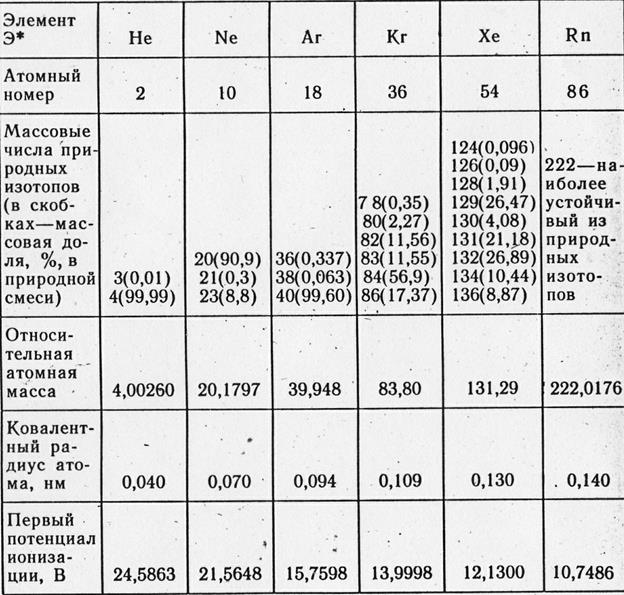
Configurarea noii bile electronice de atomi de heliu 1 s 2, cele mai mari elemente ale grupului VIII - ns 2 np 6 .
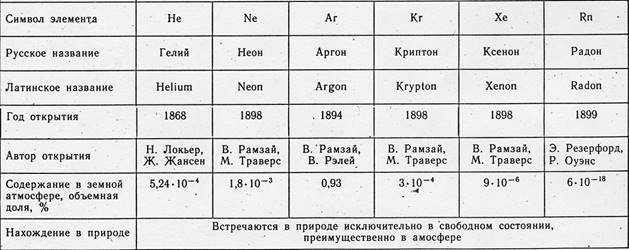
1.2 Pământ de argon.
Pe Pământ, argonul este mai puternic, dar nu singurele elemente ale acestui grup, simultan. Yogo mijloc în loc de scoarța terestră (clarke) de 14 ori mai mult, mai puțin gel și de 57 de ori mai mult, mai puțin neon. Є argon în apă, până la 0,3 cm 3 în apă de mare și până la 0,55 cm 3 în apă dulce. Tsikavo, la amurgul microfonului plutitor, argonul coastei știe mai multe, mai jos în amurgul atmosferic. Mai mult, în apă, argonul este mai frumos pentru azot... Atmosfera este capul argonului pământesc. Yogo în nіy (în spatele wagoya) 1,286%, cu 99,6% argon atmosferic - izotopul nyvazhchy - argon-40. O fracțiune și mai mare a izotopului din rujeola cu argon pământ. Timp de o oră, la trecerea la un număr mare de elemente luminoase, imaginea este gigantică - pentru a depăși izotopii luminii. Motivul acestei anomalii a fost dezvăluit în 1943. La scoarța terestră, există o potrivire strânsă pentru argon-40 - un izotop radioactiv de 40 K calorii. Cu toate acestea, numărul absolut de calorii-40 este mare, iar câteva calorii sunt unul dintre cele mai răspândite elemente de pe planeta noastră. În tone dermice de rase de incinerare, 3,1 g de calorii-40. Picătură radioactivă a nucleelor atomice caliyu-40 și două căi simultan. Aproximativ 88% din calciul-40 va scădea în beta și se va transforma în calciu-40. Ale în 12 picături de 100 (în mijloc) din nucleul de calium-40, nu este viprominuyut, ci, navpaki, un electron la cel mai apropiat nucleu de K-orbită (K-inundare). Acumularea unui electron z'єnutsya cu un proton - afirmă un nou neutron în nucleu și neutrino viprominuєuet. Numărul atomic al elementului este schimbat cu unul, iar masa nucleului este suprapusă. Deci kaliy va fi transformat în argon. Perioada pentru perioada de 40 K pentru a ajunge la mare - 1,3 miliarde de ruble. Pentru aceasta, procesul de stabilire a 40 Ar la nadra Pământului este banal și descurajantă. La faptul că argonul este „văzut” de litosferă ca urmare a proceselor vulcanice, în vivificarea și recristalizarea unor astfel de surse de apă și apă. De fapt, într-o oră aprovizionarea Pământului cu calorii radioactive a crescut dramatic - a devenit de 10 ori mai mică (ceea ce înseamnă că aprovizionarea Pământului este egală cu 4,5 miliarde de ruble). Distribuția izotopilor 40 Ar: 40 K și 40 Ar: 36 Ap în rocile stâncoase a stat la baza metodei argonului pentru determinarea valorii absolute a mineralelor. Evident, este mai veche decât rasa. Metoda argonului este cea mai importantă în ceea ce privește generația veșnică și numărul mai mare de minerale de înaltă calitate. Profesorul E.K. Gerling în 1963 a fost distins cu Premiul Lenin. Otzhe, tot sau chiar întregul Argon-40 a fost plasat pe Pământ sub formă de calia-40. Acesta este un izotop important și o dominantă a argonului pământului. Birocrat Tsim explică, înainte de vorbire, una dintre anomaliile sistemului periodic. În timp ce principiul primar al її induce - principiul mașinilor atomice - pune argonul în fața mesei în fața caloriilor. Yakby în argon, ca și în elementele susidnіh, a trecut prin izotopii de lumină (cum ar fi tse, mabut, șoareci mici în spațiu), apoi mașina atomică la argon ar avea două sau trei mensha singure ... Acum despre izotopii de lumină. Stelele sunt luate 36 Ar și 38 Ar? Ymovіrno, scho parte din atomii cich ai plimbării recreative, tobto. O bucată de argon ușor a venit în atmosfera pământului din spațiu pentru a forma planeta și atmosfera noastră. Mai mulți izotopi de lumină din argon s-au născut pe Pământ în timpul proceselor nucleare. Dar nu toate aceste procese au fost încă dezvăluite. Shvidshe pentru toate deyakі de la ei cu mult timp în urmă, cioburi au fost culese de atomi de scurtă durată - „părinți”, ale și procesele nucleare, care poninі împotriva, în care apar argon-36 și argon-38. Tse beta-decay clor-36, bombardat cu particule alfa (în minerale de uraniu) sirki-33 și clor-35:
36 17 Cl β - → 36 18 Ar + 0 –1 e + ν.
33 16 S + 4 2 He → 36 18 Ar + 1 0 n .
35 17 Cl + 4 2 He → 38 18 Ar + 1 0 n + 0 +1 e .
Mama tuturor argonului ideilor este mai clară decât pe planeta noastră. Mai ales bogate în vorbire sunt stelele fierbinți și nebuloasele planetare. Este mai bun decât argonul în spațiu, mai puțin clor, fosfor, calciu, calorii - elemente care sunt chiar mai largi decât Pământul. Argonul cosmic panuyut izotop 36 Ap și 38 Ap, argon-40 în Vsesvit este mult mai puțin. În același timp, o analiză spectrală de masă a argonului din meteoriți este în curs de desfășurare. În același timp, pentru a reconecta lățimea calibrului. Se vede, cosmosul are un calibru de aproximativ 50 de mii. după ce a dezvoltat mai puțin, mai puțin argon, apoi ca pe Pământ, este clar că caloriile sunt scorțișoară - 660: 1. Și dacă nu sunt suficiente calorii, atunci argon-40 va lua stelele?!
IIІIstoria afișării gazelor interne.
Până la sfârșitul secolului al XVIII-lea, au existat o mulțime de gaze noi. În fața lor zăceau: kissen - gaz, scho pіdtrimu gornnya; dioxid de carbon gaz - poate fi găsit cu ușurință în spatele puterii și mai primitive: câștiga apa; i, nareshty, azot, deci cuptorul nu se folosește și apa nu se consumă. Un asemenea boom a fost dezvăluit la acea oră, depozitul atmosferei, și asta, cu excepția locuinței lordului englez Cavendish, care nu a putut afla.
I vin mav privid for sumniv.
În 1785, rotsi vin zrobiv pentru a termina admiterea prostituției. Nasamper vіn vіn vіtrya vіtrya vіtrya vіtrya gaz. La suma azotului și acrișorului, am fost copleșit, mi s-a făcut o tăietură electrică. Azotul, reacționând cu acru, dând burlivi o pereche de oxizi la azot, care se găsesc în apa de băut, au fost transformați în acid azotic. Această operațiune a fost repetată bagatorazov.
Cu toate acestea, trei mai puțin decât o parte din obsyagu povitrya, luate pentru publicitate, au devenit invizibile. Păcat că întregul episod al trecutului nu este chiar stâncos.
U 1785 p. Chimistul și fizicianul englez G. Kavendish a găsit gaz nou la începutul zilei, superb de stabil. Aproximativ o sută douăzeci de părți din obsyagu povitrya au căzut în fața gazului. Ale scho tse pentru gaz, Kavendish z'yasuvati nu a ajuns. Aproximativ 107 soarta s-a ghicit despre asta, de când John William Stratt (Lord Rayleigh) l-a frecat pe aceeași casă, ținând cont că azotul este mai important, mai puțin azot, viziuni din spoluk. Necunoscând o explicație sigură a anomaliei, Stafeta, prin jurnalul „Nature”, a apelat la colegii săi-naturaliști să propună deodată să se gândească și să încerce să rezolve problema motivelor... mai importante, scăderea azotului, iar în marginea chimiei inerte. Dacă duhoarea a venit de la știrile publice despre atac, atunci ostilitatea a fost făcută într-un mod viclean. Bagaty arăta ca un neymovirny, așa că câteva generații de studenți, în timp ce urmăreau mii de analize, s-au uitat la partea lor din depozit și îmi voi aminti așa! Până la vorbirea, în aceeași zi și an, 13 secera, născută în 1894, argonul și-a tăiat imaginea, care în nuc înseamnă „nu mare”. Yogo proponuvav Dr. Medan, ca un cap pe gard. Tim este o oră de nimic minunat prin faptul că argonul a atârnat până acum din toată lumea. Adzhe în vinurile naturii nu îmi arată nimic! S-ar putea pune o paralelă cu energia nucleară: vorbind despre lucruri dificile, A. Einstein, după ce a respectat că nu este ușor să recunosc bagacy, din moment ce nu este ușor să-mi câștig banii... Ale nu lipsite de vitrați morali: chin prin atacurile colegilor (mai ales chimiști). Impresii mari, victorie și în realizări fizice de rezultate semnificative, pentru scho în 1904 p. Bouv a fost distins cu Premiul Nobel. Todi este la Stockholm pentru că îl cunosc pe Ramzaєm, care a scăpat de ziua aceea Premiul Nobel pentru deschiderea gazelor nobile, inclusiv argonul.
 |
În stânca aprigă din 1895, Razmay pe frunzele meteorologului londonez Maurs, pentru copii despre amintirile geologului american Gillebrand, care fierbea la acizii acizi, puterea uraniului a fost arătată puterii gazului. Pe măsură ce se găsește mai mult uraniu în minerale, se observă mai mult gaz. Gillebrand lăsând-o să plece, ca gazul є cu azot. — Poate argon? - hrănirea autorului foii.
Nezabarom Rosemay și-a trimis prietenii la farmaciile londoneze pentru uraniu. Bulo a cumpărat 30 de grame de kleveite, iar în acea zi Rosemay, împreună cu prietenul său Matthews, a cumpărat o sticlă de centimetri cubi de gaz. Rosemay a furnizat gaz pentru dozarea spectroscopică. Win lovind yaskravu zhovtu liniyu, tot merg la linia de sodiu și la aceeași oră o văd în spatele poziției mele la spectru. Rosemay cartea clădirii, apoi ridicați spectroscopul, curățați-l și, cu cunoștințe noi, dezvăluie o nouă linie, care nu a scăpat de linie. Rosemay aruncă o privire asupra spectrului tuturor elementelor. Nareshty câștigă ghicit despre ghicitoarea liniei din spectrul coroanei somnoroase.
 |
În 1868, a început ora întunecării somnoroase, predicatorul francez Zhansen și englezul Lok'or vyavili la spectrul protuberanțelor somnorose yaskravu zhovtu liniyu, care nu apărea în spectrul terestru al luminii dzherel. În 1871, a apărut Lok'ar visloviv, care nu se potrivea cu întregul spectru al vorbirii neobișnuite de pe Pământ.
Vin numind elementul ipotetic heliu, tobto „adormitor”. Ale pe pământ nu a explodat. Fizica și chimie în care nu m-am prins: pe Sontsi, mișcându-ne, chemându-ne, e apă care merge după heliu.
Ce anume este heliul în mâinile tale? Rosemay poate fi cel mai bun compozitor din comunitate, chiar dacă simți că a fost confirmat de spectroscopistul de acasă al lui Crookes. Rose poate primi gaz a doua zi și scrie despre cei care cunosc noul gaz, numele lor sunt krypton, nuc înseamnă „prikhovaniye”. Telegrama de la Crooks spunea: „Crypton є heliy”.
2.3 Krypton.
 |
Până în 1895, roca a fost produsă de două gaze interioare. Era clar că între ei era un singur gaz, puterea a ceea ce Rosemay a descris în spatele fundului lui Mendelev. Lecoq de Boisbaudran, transferat la navi de gaz neperturbator - 20.0945.
Din neatenție, după ce am văzut știrile ultimelor știri, în ultima oră, Linde din Genmania și Hempson din Anglia nu au luat brevet pentru mașină peste noapte, dar nu l-am primit.
Tsya car nemovbi Bula este special conceput pentru detectarea gazelor interne. Principiul її ї dії învățarea pe un fel de manifestare fizică, parcă stors, apoi crește repede, este rece. Ne vom răci noaptea, vom răci o nouă parte a zilei, vom veni la mașină etc.
Viparuvavshih tot azotul și kissen, Rosemay rіdke povіtrya, scho a revărsat, ținând un contor de gaz. Dacă te-ai gândit să cunoști heliu într-un loc nou, te-ai întrebat despre el, astfel încât gazul să fie vaporizat mai mult, mai puțin acid și azot. După ce purificăm gazul din contorul de gaz din casă, acrim azotul și cunoscând spectrul, care nu a mai văzut nicio linie până acum.
Dali Rosemay a cheltuit 15 litri de argon la sticlă de către micuțul bricolaj. Pentru a cunoaște gazul interior, în spatele rozariului, lumina, argonul inferior și criptonul, Razmay ridică primul port de vaporizare a argonului. Vyyshov un nou spectru de linii strălucitoare-chervony. Rosemay a numit viziunea neonului de gaz, care în nuc înseamnă „noviy”.
Dali Rosemay a cheltuit 15 litri de argon la sticlă de către micuțul bricolaj. Pentru a cunoaște gazul interior, în spatele rozariului, lumina, argonul inferior și criptonul, Razmay ridică primul port de vaporizare a argonului. Vyyshov un nou spectru de linii strălucitoare-chervony. Rosemay a numit noul gaz neon, care înseamnă „nou” în nuc.
2.5 Xenon.
În 1888, pomichnik razmaya Travers, după ce a rămas în mașină, a dat o temperatură de -253 0 С. Bulo a recunoscut toate gazele, cu excepția criptonului. Xenonul („extraterestru”) era deja cunoscut în criptonul nerafinat. Pentru a tăia 300 de centimetri cubi de xenon, am reușit să spargem 77,5 milioane de litri de energie atmosferică în 2 ani.
De asemenea, se spune că heliul este prezent în mineralele de uraniu. Există mai mult în întărirea uraniului, mai mult în gel. Rosemay nu știa cum să cunoască legătura dintre uraniul rău și heliu, care nu ajungea în el. Răspunsul a venit din lateral; Vona Bula cu indicatii de radioactivitate.
Viyavili, care este un discurs asemănător gazului, se numește emanație. 1 gram de radiu pe zi pentru un milimetru cub de emanație. În 1903, Rozmay și Vidomy Fizik Soddi au început munca de emanare. Duhoarea privării lor ordonate a 50 de miligrame de bromură de radiu; o oră miros de trocha mai mult de 0,1 milimetru cub de emanație.
Pentru vizitator, Robit Rosemay a creat un vagi simpatic, arătând câteva milioane de bucăți de grame. Nevzі prelіdniki z'yasuvali, emanația є rămâne un reprezentant al familiei gazelor interne.
Nu am intrat în spectrul emanației. Yakos, după ce a umbrit tubul timp de câteva zile, a pus duhoarea în spectroscop;
Întregul fapt de a confirma aprobarea lui Rutherford și Soddy se referă la cei care nu sunt reconfigurați radioactiv asociat cu reconfigurarea atomilor. Radio, trecând, transformându-se în emanație și văzând nucleul unui atom cu heliu. Un element este convertit în unul.
Vcheny a devenit un zel, de ce heliul apare în materialele cu uraniu; unul dintre produsele din declinul uraniului. În 1923, conform deciziilor Comitetului Internațional de Chimie, emanația Bulei a fost redenumită radon.
III Puterea gazelor interne și a spoluk-urilor.
3.1 Puterea fizică a gazelor interne.
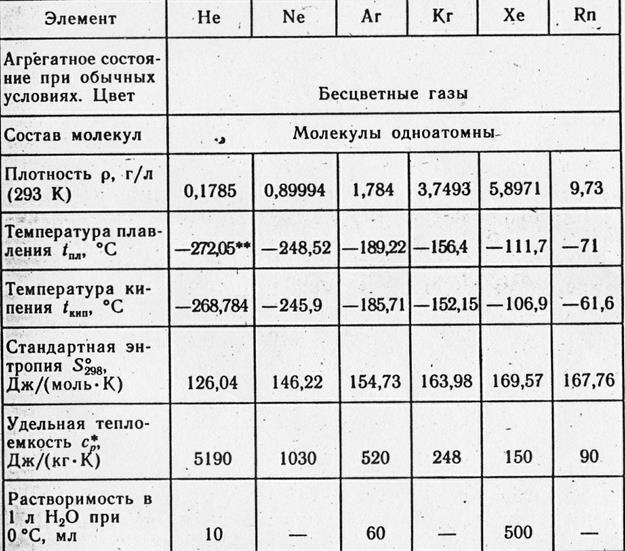
Gaze Shlyakhetnі - gaz monoatomic steril, fără culoare și miros.
Gazele inerte pot avea o conductivitate electrică mai mare în cazul unor gaze; atunci când fluxul trece prin ele, fluxul se va lumina puternic: gelul este o lumină strălucitoare, care este cumva conectată la un spectru simplu. neon în foc este un nume de vierme cu lumină, fragmente din cea mai frumoasă linie se află în centrul spectrului.
Caracterul inflamat al moleculelor atomice ale gazelor interioare este indicat de faptul că gazul interior este punctul cel mai scăzut de creștere și îngheț, cel mai jos este gazul cu corpul molecular însuși. Argonul este cel mai ușor din grupul de gaze energetice importante. Vін important pentru o viraj în 1,38 ori. Ridina crește la - 185,9 ° C, mai tare la - 189,4 ° C (într-o scurgere de prindere normală).
Sub formă de heliu și neon, este bine să fie adsorbit pe suprafețele particulelor solide și să se spargă lângă apă (3,29 cm 3 la 100 g apă la 20 ° C). Este și mai frumos să găsești argon în bagatokh organic ridynah. Este practic nerezonabil pentru metale și nu pentru difuzarea lor.
3.2 Autoritățile chimice ale gazelor interne.
Multă vreme, nu au existat minți pentru care privirile nobile să poată intra în chimie. Duhoarea nu s-a prefăcut a fi niște spoluks obraznici. Cu alte cuvinte, valența їхnya este zero. În momentul producției, un nou grup de elemente chimice a fost actualizat la zero. Activitatea chimică minimă a ziarelor nobiliare este explicată prin configurația ascuțită de opt electronice a mingii electronice. Polarizarea atomilor în creștere datorită creșterii numărului de bile electronice. Otzhe, nu vei putea petrece o oră trecând de la heliu la radon. În același timp, există o mare schimbare și reacție în construirea nobilității.
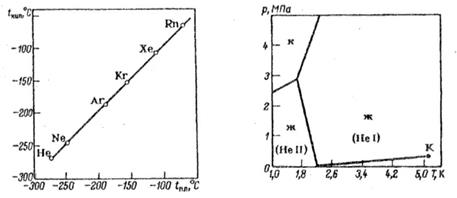

Așadar, încă din 1924, a început să curgă ideea că unele gaze energetice importante (germeni, fluor și clorură de xenon) erau stabile termodinamic și puteau fi alimentate de minți rele. De nouă ori mai târziu, ideea a fost adoptată și dezvoltată de teoreticieni - Pauling și Oddo. Introducerea structurii electronice a cochiliilor în kripton și xenon din pozițiile mecanicii cuantice a condus la ideea că gazele pot fi făcute cu fluor. Se știa și experimentatorii, deoarece au încercat să reconsidere ipoteza, dar încă o oră, au fost puse până la ultima, iar fluorura de xenon nu este folosită. Drept urmare, toți roboții din întregul galuzzi au fost prinși, iar gândul la inerția absolută a gazelor nobiliare a fost afirmat rezidual.
Cu toate acestea, în 1961, rotsi Bartlett, cercetător al uneia dintre universitățile din Canada, în puterea hexafluorurii de platină, cu jumătate de fluor activ, mai mic în sine, având instalat potențialul de ionizare în xenon inferior (12 în Timp de o oră, configurați-o cu hexafluorură de platină din partea de jos a magazinului O 2 PtF 6 ... Când este încălzit în vid, XePtF 6 pâlpâie fără a se desface, în apa pe care o hidratează, xenonul este vizibil:
2XePtF 6 + 6H 2 O = 2Xe + O 2 + 2PtO 2 + 12HF
Roboții ofensivi ai lui Bartlett au fost lăsați să stea, că xenonul a fost depus din mintea reacției în două jumătăți cu hexafluorură de platină: XePtF 6 și Xe (PtF 6) 2; în caz de hidroliză este inclus unul dintre cele mai delicioase produse. După ce a trecut peste, apoi xenonul a intrat efectiv într-o reacție cu hexafluorura de platină, Bartlett, după ce a prezentat un raport suplimentar în 1962, a publicat un articol în revista „Proceedings of the Chemical Society” atribuit criteriului zdrobit de el. Statutul a stârnit un interes magnific, dacă i s-a pus multă chimie cu o neîncredere inacceptabilă. Timp de mai bine de trei ani, experimentul lui Bartlett a fost repetat de un grup de preliminarii americani pe un chol z Chernik în Laboratorul Național Argonne. În plus, duhoarea a fost prima care a sintetizat spoloi analogi de xenon cu hexafluoruri de ruteniu, rodiu și plutoniu. Așadar, gloanțele arată primele cinci până la cinci cu xenon: XePtF 6, Xe (PtF 6) 2, XeRuF 6, XeRhF 6, XePuF 6 - mitul despre inerția absolută a gazelor nobiliare în dezvoltarea vremurilor noi.
Suma de gaz (1 parte de xenon și 5 părți de fluor) a fost plasată într-un vas de nichel (nikel foarte stabil la fluor) și a fost încălzită cu un menghin destul de mic. Un an mai târziu, vasul a fost răcit rapid, iar gazul, care se vărsase în cel nou, a fost pompat și analizat. Fluorul acela. Tot xenonul a reactionat! Au spart vasul și vyavili la noul cristal XeF 4. Tetrafluorura de xenon a apărut dintr-o singură bucată, iar molecula are forma unui pătrat cu ioni de fluor de-a lungul tăieturii și cu xenon în centru. Tetrafluorura de fluor xenon mercur:
XeF4 + 2Hg = Xe + 2HgF2
Platina poate fi fluorurată la un preț, dar nu o putem compara decât cu fluorul din apă.
Este posibil să eliminați nu numai XeF 4, ci doar fluor-XeF 2 XeF 6.
Chimiștii Radianske V.M. Khutoretskiy și V.A. Pentru proponarea lor prin intermediul unei metode, suma de xenon și fluor (la un raport molecular de 1: 1) este introdusă într-un vas dintr-un nichel din oțel inoxidabil, iar atunci când presiunea este împinsă până la 35 atm, este reparată o reacție de mimă.
XeF 2 - fluorură de xenon unică, care poate fi tăiată fără a utiliza fluor elementar. Win se stabilește cu o descărcare electrică de xenon și tetrafluorură în carbon. Sinteză dornică, tare și directă. Chiar și cel mai pur XeF 2 se stinge, ca și cum suma de xenon și fluor este copleșită de ultraviolete. Rezistența la difluorura în apă este scăzută, iar rezistența la aceasta este cel mai puternic agent oxidant. Probabil vіn samorozladaєtsya pe apa cu xenon, kisen și fluorură; răspândindu-se mai ales rapid undeva lângă centrul bălții. Difluorura are un miros specific puternic. Mare interes teoretic în metoda de sinteza de difluorura de xenon, umplere pentru injectarea de viprominuvannya ultraviolete pe suma gazelor (pentru o cantitate de aproximativ 2500-3500 A). Viprominuvannya wiklicaє scindarea moleculelor de fluor în atomi vilny. În cazul unei poliagaє, motivul pentru care se afirmă difluorura este că fluorul atomic este supra-înalt activ. Pentru îndepărtarea XeF 6, valorile necesare sunt: 700 ° С і 200 atm. În astfel de minți de xenon și fluor (de la 1: 4 la 1: 20), practic tot xenonul este convertit în XeF 6. Hexafluorura de xenon este superficial activă și se pliază cu vibuch. Vinul poate fi ușor reacționat cu fluorurile de metale străine (crim LiF):
XeF 6 + RbF = RbXeF 7,
ale la 50 ° C, syl se va plia:
2RbXeF 7 = XeF 6 + Rb 2 XeF 8
A existat, de asemenea, o sinteză a fluorurii de lichen de calitate alimentară XeF 8 la temperaturi sub minus 196 ° C.
Sinteza primelor spoluks de xenon prin punerea în fața chimiștilor a hranei despre gazele interioare din sistemele periodice. În fața gazelor nobile, am văzut în vecinătatea grupului zero, dar s-a făcut tot anunțul despre valența acestuia. Dacă xenonul a intrat într-o reacție chimică, dacă a devenit un tip de fluor, valența xenonului este de până la opt (și, în același timp, este necesar să se folosească energia carcasei electronice), se adaugă gazele inerte. la faza a VIII-a. Grupul nulului a încetat să mai existe.
Xenonul Zmushiti intră într-o reacție fără participarea fluorului (unele dintre ele spoluch) fără a ajunge nicăieri. Eliminați fără efort fluorurile din xenon. Discursul poate duce la reacția clădirii. Naykrasche vivcheno schimbul de fluoruri de xenon cu apa. Hidroliza XeF 4 într-un mediu acid până la aprobarea oxidului de xenon XeO 3 - cristale fără bare, care pot fi distribuite pentru utilizare. Molecula XeO 3 are structura unei piramide triunghiulare stropitoare cu un atom de xenon în vârf. Tse z'єdnannya vkray nestiyke; când forța vibuch-ului este răspândită, este aproape de impulsul vibuch-ului TNT. Câteva sute de miligrame de XeO 3 au fost sparte în sicrie. Nu viklyucheno, într-o oră, trioxidul de xenon va fi învingător, yak vibukhovu discurs diii, scho zdrobire. O astfel de vibuchivka a unui glonț ar fi mai manuală, astfel încât toate produsele unei reacții vibuchiv sunt gaze. Este și mai scump ca xenonul methi trioxid să scape de el - este și mai puțin costisitor pentru xenonul într-o atmosferă, mai puțin aur în apa de mare și este greu de văzut. Nagadaєmo, pentru îndepărtarea a 1 m3 de xenon, va fi necesară reciclarea a 11 milioane m3 de pulbere. Acidul nestabil al xenonului hexavalent H 6 XeO 6 este similar cu trioxidul și se stabilește ca rezultat al hidrolizei XeF 6 la 0 °
XeF 6 + 6H 2 О = 6HF + H 6 XeO 6
Chiar înainte de produsele lanțului de reacții, shvidko dodati (OH) 2, vipadaє sediment amorf Ba 3 XeO 6. La 125 ° C, vinul se depune pe oxid, xenon și oxigen. Saruri analoge Otrimano-xenonat de sodiu si calciu. Când ozonul atinge intervalul de XeO3 în hidroxid de sodiu molar, se stabilește concentrația acidului acid și a xenonului Na4XeO6. Perxenonatul de sodiu poate fi văzut sub formă de hidrat cristalin fără bare Na4XeO6 · 6H 2 O. Înainte ca perxenonații să fie aprobați, induceți hidroliza XeF 6 în hidroxizi de sodiu și calorii. Pe lângă Na 4 XeO 6 solid, acesta poate fi curățat cu nitrat de plumb, amestecat cu uraniu, inclusiv următoarele tipuri de perxenonați: PbXeO 6 і (UO 2) 2XeO 6 în aceeași culoare și Ag 4 XeO 6 - negru. Sărurile analoge dau calciu, litiu, cesiu, calciu.
Oxidul, care transformă acidul acid în xenon, este distilat sub formă de Na4Xe06 cu acidul sircanic anhidru răcit. Tse chotirikis xenon XeO 4. În nіy, yak і în octafluorura, valența xenonului este egală cu opt. Chotirikis solid la o temperatură de 0 ° C se descompune în xenon și muselină și asemănător gazului (la temperatura camerei) - în trioxid de xenon, xenon și mussen. Molecula XeO 4 are forma unui tetraedru cu un atom de xenon în centru. Există două moduri de a trece prin drenajul hexafluorurii de xenon; într-un vipad pentru a introduce tetraoxifluorura XeOF 4 іnshomu - deoxifluorura XeO 2 F 2. Sinteza directă a elementelor pentru a produce oxifluorura XeOF 2 până la aprobare. Toate discursurile solide de neprețuit, stigmatizarea minților rele.
Duzhe Tsikava a primit recent o reacție de difluorură de xenon cu НС1O 4 anhidru. Ca urmare a unei serii de reacții, este adoptat un nou tip de xenon XeClO 4 - un agent de oxidare super-strâns, care este cel mai puternic dintre toți perclorații.
Se sintetizeaza si cu jumatate de xenon, care nu se razbuna pe acru. Mai important, sub-sărurile, produsele interacțiunii fluorurilor din xenon cu fluorurile de surmi, mish'yak, bor, tantal: XeF 2 SbF 5, XeF 6 AsF 3, XeF 6 BF 3 și XeF 2 2TaF 5. I nareshty, tip vorbire confuză XeSbF 6, stil pentru temperatura camerei și XeSiF 6 - complex instabil.
La chimiștii comandați є adăugați cantități nesemnificative de radon, ridicați-vă departe, deci se datorează și fluorului, care face ca fluorul să nu fie volatil. Pentru krypton și vivcheni difluorura KrF2 și tetrafluorura KrF 4 pentru putere, care poate fi găsită cu jumătate din xenon.
3.3 Respingerea argonului.
Atmosfera Pământului urmează să răzbune 66 · 1013 tone de argon. Argonul nu a contat, mai mult argon este suficient de devreme pentru a se transforma în atmosferă și, atunci când este învingător, nu se încrede în vreo schimbare fizică sau chimică. Vinyat-ul devine și mai nesemnificativ cantități de izotopi în argon, astfel încât se dovedește a fi aruncat în reacțiile nucleare ale unor noi elemente și izotopi. Eliminați argonul ca produs secundar atunci când alcoolul este adăugat la oxigen și azot. Zvvychay vikoristovuyt pertrozdiluvalny aparati dvorazovy rectifikatsii, care este stocat din colonia inferioară a unei menghine înalte (podul frontal), colonia superioară. menghină joasă cea a condensatorului intermediar-viparnik. Kinets kinets azotul este introdus de sus, iar kissen - din spațiul de deasupra condensatorului. Volatilitatea argonului este mai mare, mai puțin acidă, mai puțin decât mai puțin, mai puțin azot. Această fracțiune de argon este luată în punctul, care este situat aproximativ la a treia înălțime a coloniei superioare, și este adusă într-o coloană specială. Depozit pentru fracția de argon: 10 ... 12% argon, până la 0,5% azot, rasht - kissen. În colonia „argon”, adusă la aparatul principal, se spală argonul cu o casă 3 ... 10% acru și 3 ... 5% azot. Purificarea ulterioară a argonului „alb” trece la acid (mod chimic sau adsorbție) și la azot (rectificat). La scară industrială, argonul poate fi spălat cu o puritate de până la 99,99%. Argonul este, de asemenea, aruncat de la intrarea amicus vyrobnitstva - din azot, dar s-a pierdut din această cauză, deoarece cea mai mare parte a fost numită apă. Argonul este folosit pentru transportul în cilindri de 40 de litri, care sunt împodobiți cu culori gri din cauza smog-ului verde și a scrisului verde. Viciul lor este de 150 atm. Este mai economic să transporti gazul argon, mai ales, vasul Dewar și rezervoarele speciale. Radioizotopii de argon dintr-o singură bucată sunt eliminați în cazul detectării anumitor izotopi stabili și radioactivi (37 Cl, 36 Ar, 40 Ar, 40 Ca) de către protoni și deuteroni, precum și în cazul neutronilor asistați. produse care au fost produse în reactoare nucleare. Izotopii 37 Ar și 41 Ar pot fi detectați ca indicatori radioactivi: mai întâi - în medicină și farmacologie, celălalt - în cazul fluxurilor de gaze preexistente, eficiența ventilației și în știința inteligentă. Ale, viclean, nu aspira argonul de pe apă.
3.4 Activitatea fiziologică a gazelor interne.
Desigur, a fost ochikuvati, a fost atât de inerte din punct de vedere chimic discursuri, precum gazul inert, nu sunt vinovate de băut și de organisme vii. Ale tse nu este așa. Inspirația de gaze energetice vishny (este comun pentru sumy cu acru) pentru a aduce o persoană în tabără, suplimentată cu alcool. Efectul narcotic al gazelor interne se acumulează în gama țesuturilor nervoase. Chim vishche energie atomică inertă la gaz, tim din ce în ce mai mult și din ce în ce mai puternic și mai narcotic.
Acum despre injectarea de argon pe un organism viu. La inhalarea unor sume din 69% Ar, 11% azot și 20% aciditate sub strânsoarea de 4 atm, are loc anestezia, pe măsură ce creșterea devine mai puternică, mai mică la inhalare, sub strânsoarea prizului. Anestezia este mittєvo cauzată de supresia argonului. Motivul este nepolaritatea moleculelor de argon, presiunea argonului în țesuturile nervoase. Biologii viyavili, că argon cu creșterea roselin. Pentru a naviga în atmosfera de argon pur, orez, porumb, ogirkiv și zhyta wicked aburi. Tsibulya, morcovii și salata verde cresc bine în atmosferă, care pot fi depozitate în 98% argon sau mai puțin de 2% acru.
IV Stagnarea gazelor interioare.
Geliy este un important dzherel al temperaturilor scăzute. La o temperatură de heliu rar, degradarea termică a atomilor și electronilor electrici din corpurile solide este practic în afara drumului, ceea ce permite dezvoltarea multor manifestări noi, de exemplu, supraprovidența într-o moară solidă.
Heliu asemănător gazului vikoristovuyat yak gaz ușor similar cu sacii uscati. Oskilki vin este incombustibil, poate fi adăugat la carcasa dirijabilului.


Deci, deoarece heliul este mai bun în sânge, mai puțin azot, există o mare cantitate de heliu care stagnează în mințile răi pentru a lucra într-o strângere, de exemplu, cu găuri de mare, cu tuneluri sub apă deschise și cu echipament. În cazul decompresiei vikoristanny heliului (o viziune a gazului evacuat din sânge), scafandru are o mulțime de dureri, există o boală mai puțin severă, cum ar fi anestezia cu azot este o sursă de apă permanentă și nesigură. Vâscozitate scăzută pentru persoanele care suferă de crize de astm și în caz de îmbolnăvire în creștere a persoanelor bolnave.
Heliu vikoristovuyak ca mijloc interior pentru încălzirea arcului, în special magneziu și acel aliaj, atunci când sunt eliminate Si, Ge, Ti și Zr, pentru răcirea reactoarelor nucleare.
Інші stocarea heliului - pentru masticarea cu gaz a rulmenților, pentru detectoare de neutroni (heliu-3), termometre cu gaz, spectroscopie cu raze X, pentru asigurarea energiei, pentru pompe de mare energie. În vârful celorlalte gaze nobile, heliul este vicios la ultimele reclame cu neon (la tuburile cu descărcare în gaz). Heliul Ridky este excelent pentru răcirea plafonurilor magnetice, aderând la particule și anexe. Aspirarea neimplicată a heliului ca agent de răcire є procesul de consum neîntrerupt de 3 He și 4 He pentru setarea și scăderea temperaturilor mai mici de 0,005 K
Zonele care depozitează xenon nu sunt potrivite pentru o oră. Lyudina vikoristovu și її ії ії ії ії ії ії іѕ este un miracol ї іtnіtnіstnіt de a rezolva reacția cu fluor. La svitlotekhnіtsі zіznannya zdobul lămpi cu xenon vysokogo menghină. Astfel de lămpi au o descărcare cu arc la xenon, dar într-o prindere la câteva zeci de atmosfere. Lumina din lămpile cu xenon apare imediat când sunt aprinse, dar există un spectru clar și neîntrerupt - de la ultraviolet la regiunea infraroșu apropiat. Xenon creep în medici - cu stări fluoroscopice ale creierului. Terci de iac și barit, care stagnează cu iluminarea intestinală, xenonul se agață puternic de viprominuvannya cu raze X și ajută suplimentar să cunoască mizeria. În același timp, nu este deloc timid. Izotop activ al elementului nr. 54, xenon - 133, vikoristovuyut la eficiența funcțională avansată a piciorului și a inimii.
Când argonul este suflat prin oțel, acesta poate vedea gazele incluse. Voi reduce puterea metalului.
Din ce în ce mai multe zastosovutsya arc electric de încălzire în mijlocul de argon. Într-un jet de argon, puteți lumina subtilitățile virobiului și ale metalului, care erau importante înainte. Nu va fi prea mult să spunem că un arc electric într-o atmosferă de argon a revoluționat tehnologia metalelor. Procesul s-a accelerat rapid, a existat posibilitatea de a tăia foile de metale refractare. Arcul de argon este suflat prin argon (în cazul apei), marginile sunt înfășurate și electrozii de wolfram sunt fabricați din oxid, nitrură și alte margele. O oră, șterg mânerul și concentrez arcul pe o suprafață mică, prin temperatura din zonă atingând 4000-6000 ° С. Atunci când este ars într-un jet de argon, nu este consumat în fluxuri și electrozi, iar apoi, în curățarea cusăturii de zgură și surplus de flux.
Neon și argon vikorizovyutsya ca în lămpile de neon și lămpile de o zi se potrivesc cu Krypton pentru a reaminti lămpile vii cu ajutorul schimbării vaporizării și îmbunătățirii calității firului de tungsten. Xenonul amintește lămpilor de cuarț de o menghină înaltă, cu cele mai necesare dzherels de lumină. Heliul și argonul pot fi folosite pentru laserele cu gaz.

Lista literaturii Victoriei
1. Petrov M.M., Mikhilyov L.A., Kukushkin Yu.M. "Chimie anorganică"
2. Guzey L.S. Prelegeri de la chimie ieșită din cutie "
3. Akhmetov NS „Zagalna și chimia neorganică”
4. Nekrasov B.V. „Chimie Pidruchnik zagalnoy”
5. Glinka N.L. „Chimia Zagalna
6. Hodakov Yu.V. „Zagalna și chimia neorganică”
Vidkrittya:
U 1893 p. respectul fiert pentru distribuția azotului din dietă și a azotului, posedat în timpul distribuției spoluks-ului de azot: un litru de azot din orice motiv este important 1,257 g, iar cel scos pe cale chimică - 1,251 r. De dragul mobilierului misterios, s-a demonstrat că, având în vedere toată aciditatea azotului, un mic surplus (aproape de 1%), care nu a reacționat chimic, nu a ieșit din el.
Apariția unui nou element, numit argon (nuc - nondialny), reprezentat printr-o astfel de ordine „curățenia a treia zecimală”. Greutatea moleculară a argonului este de 39,9 g/mol.
Gazul inert, care vine o oră mai târziu, - heliu („somnolos”), a fost văzut mai devreme pe Sontsi, sub Pământ. Metoda analizei spectrale, care a fost defalcată în anii 50 ai secolului trecut, a devenit posibilă.
Printr-un mic mesaj stâncos către argon și heliu (născut în 1898), au fost văzute încă trei gaze interioare: neon ("noviy"), krypton ("prikhovaniye") și xenon ("extraterestru"). Naskіlka important, se poate observa că, aproximativ 1 m 3 de crepuscul, aproximativ 9,3 litri de argon ar trebui înlocuiți cu 18 ml de neon, 5 ml de heliu, 1 ml de cripton și 0,09 ml de xenon.
Gazul interior rămas - radon bulo vidkrito 1900 r. minerale schodo deyakim Trecerea din atmosferă la o privare de 6-10 -18% pe volum (care este legată de 1-2 atomi într-un centimetru cub). Bulo pіdrahovano, astfel încât întreaga atmosferă pământească să se răzbune pe privarea de 374 de ani de radon.
Autoritati fizice:
Toate gazele fără energie sunt stocate în molecule monoatomice. Podil gaze inerte runtutsya pe opiniile autorităților fizice їkh.
Gazele inerte fără bariere nu miros. Aveți o cantitate mică de duhoare prezentă în fiecare masă. Gazele inerte nu sunt întrerupte. Cu toate acestea, atmosfera cu concentrația crescută de gaze energetice și scăderea rezultată a concentrației de acid poate pune presiune asupra oamenilor, până la pierderea dovezilor și moartea. În urma căderii oamenilor după ora de întoarceri în argon.
|
Temperatura de topire, ° С |
||||||
|
Temperatura balotului, ° С |
Cantitatea de căldură, necesară pentru transferul vorbirii dintr-o moară solidă în pat, este căldura de topire, iar pentru transferul de la moara tare la una asemănătoare aburului - căldura de vaporizare. Ofensa la marime, lasa-l sa fie suportat inainte de tranzitii, astfel incat sa se faca intr-o prindere normala. Pentru gazele interioare, mirosul poate fi după cum urmează (kcal / g-atom):
|
Căldura de topire |
||||||
|
Căldura viparovannya |
Fundul camerei temperatura critica
Gaze inerte și vicii, care sunt necesare și suficiente pentru transferul la aceleași temperaturi de la o moară asemănătoare gazului la una mică, - menghină critică:
|
Temperatura este critică, ° С |
||||||
|
Aderență critică, atm |
Nutriția atomicității moleculei de argon a fost încălcată dintr-o teorie cinetică suplimentară. De fapt, cantitatea de căldură, așa cum este necesară pentru vitratețe pentru a încălzi o moleculă gram în gaz cu un grad, pentru a depune unii dintre atomi din acea moleculă. În cazul schimbului continuu, molecula gram a unui gaz monoatomic vimagan 3 fecale, diatomic - 5 cal. Pentru argon, dând 3 fecale, a influențat monoatomicitatea moleculei sale. Acestea sunt denumite și cele mai mari gaze interne.
Gelіy buv ostanіm іf gaz translations u rіdky that firm stan. Ca urmare a expansiunii la temperaturi normale, heliul nu se răcește, ci mai degrabă se încălzește. Dacă este mai mică de -250 ° C, este bine să începeți. Sună ca o experiență de vaping, așa că procesul extravagant de recuperare va stagna până când se va răci prea mult. Pe de altă parte, temperatura este critică, heliul ar trebui să fie scăzut pe margine. Puterea ciches-ului mediului este prietenoasă, rezultatele atunci când robotul cu gel sunt gloanțe sunt îndepărtate din procesul de rehidratare prin metoda de operare cu apă fierbinte, coryzing cu vipar, care poate fi folosit doar pentru a răci gelul până la temperaturile cerute. Otrimaty ridky gelіy a mers înainte în 1908, heliu solid-y1926 p.
Autorități vesele:
Gazele inerte se caracterizează printr-o frecvență mai mare (He, Ne, Ar) sau mai mare (Kr, Xe, Rn) a cantității de activitate chimică. În sistemul periodic, mirosurile formează un grup special (VIII). Producția discretă de gaze în aer liber a fost aprobată de ei în sistemul periodic grup nou Bula se numește zero, iar valența acestor elemente este zero, astfel încât au activitate chimic activă. Un astfel de nume stagnează adesea într-o oră dată, protest, conform legii periodice, este mai corect să se respecte grupul de gaze interioare până la al optulea, unele dintre elemente nu sunt reparate, ci să se termine.
Vizibilitatea gazelor inerte importante cu mai multă inerție chimică a fost lipsită de 1962 p. Se pare că duhoarea a fost construită cu cel mai activ metal - fluor (dacă nu îl aveți). Xenonul (și radonul) reacționează ușor, criptonul este mai important. Otrimano XeF 2, XeF 4, XeF 6 și KrF 2 cu consum redus de energie. Duhoarea duhoarei є scurgerile sterile ale vorbirii de cristal.
Difluorura de xenonă(XeF 2) -Se stabilește de ziua luminii zilei Xe și F 2 la n.o. Există un miros plictisitor caracteristic. Pentru aprobarea moleculei, atomul de xenon trebuie alimentat de la 5s 2 5p 6 la cea mai joasă stare bivalentă 5s 2 5p 5s 1 - 803 kJ / mol, până la 5s 2 5p 5 6p 1 -924 kJ / mol, 25s 2 5p 1 6 ml.
Xe + F2 → XeF2
Concentrația apei este de 0,15 mol/l. Roschin є și mai puternic oxidant. Rozchin să prezinte schema:
XeF2 + H2O → HF + Xe + O2
Xenontetrafluorura Pentru a se afirma din cuvinte simple, reacția este puternic exotermă, este cea mai bună dintre toate fluorurile.
XeF4 + 2Hg = 2HgF2 + Xe
XeF4 + Pt = PtF4 + Xe
Reacția Yakisna la tetrafluorura de xenon :
XeF 4 + 4KI = 4KF + 2I 2 ↓ + Xe
Tetrafluorura de xenon este pliată în spatele schemelor:
3Xe 4+ → Xe 6+ + 2Xe 0 (în mijlocul acru).
Xe 4+ → Xe 0 + Xe 8+
Fără xenonexafluoruri, vidomie în trei modificări cristaline. La 49 ℃, se transformă într-o zhovtu rіdina, când se întărește, nu va mai deranja. Pari Mayut Blido-Zhovte Zabarvlennya. Rabatați din vibuch. De la începutul conversației:
XeF6 + H2O → 2HF + OXeF4
OXeF 4 fara barvna ridina, cladire mai putin reactionara, inferior XeF 6
Cu o hidroliză suplimentară, puteți elimina trioxidul de xenon:
XeF6 + 3H20 → XeO3 + 6HF
XeO 3 este vibuchovina fără bare, deci poate fi distribuită la fiecare pas. Pentru a cădea cu un vibuch, ale cu o încălzire îngrijită la 40 de grade pentru Celsius, are loc o reacție:
2XeO 3 → 2Xe + 3O 2
Є acid, care este formal similar cu oxidul dat-H 2 XeO 4.
3XeF 4 + 6Ca (OH) 2 → 6CaF 2 ↓ + Xe + 2H 2 XeO 6
În lumina puternică a lunii Xe 6+ dismuth:
4Xe 6+ → Xe 0 + 3Xe 8+
Difluorura în kripton- letki bezbarvnі cristale vorbirea este activă chimic. La temperaturi în schimbare, întindeți-vă cripton fluor ... Buv pentru prima dată otrimaniyu descărcare electrică pentru vorbire sumish, la -188℃:
F 2 + Kr → KrF 2
Așezați-vă cu apă în spatele schemei:
2KrF2 + 2H2O → O2 + 4HF + 2Kr
Stagnarea gazelor interioare:
Gazele inerte știu să facă afaceri mai profitabile este mai practic. Dimineața, rolul heliului este foarte important atunci când se elimină temperaturile scăzute, deoarece heliul rar este foarte rece. Lipsa gazului în prinderea crescândă este mult redusă, că la pornirea apei, care se scufundă lângă apă și este asigurată de slujitorii slujitori, adăpostul pentru azot este mai mare, mai scăzut în mințile normale. În momentul de față, dacă prinderea cade, azotul se descompune, iar când se văd bulbii, deseori înfundă alte vase de sânge, dăunând circulației normale a sângelui și atacând „boala”. Directorii care înlocuiesc azotul cu afecțiunile cu heliu se vor slăbi rapid pe măsură ce cantitatea de heliu din sânge devine mai puțin predispusă la heliu, care este recunoscut în special pentru aderența în creștere. Robotul în atmosfera de răsucire „gel” permite scafandrilor să coboare pe un glibini mare (peste 100 m), ceea ce înseamnă termenul podovzhuvati perebuvannya sub apă.
Deci, deoarece competența unei astfel de băuturi este de aproximativ trei bărbați, competența unui nagato extravagant, dihotomic este mai ușoară. Tsim a fost informat despre marea semnificație medicală a băuturii cu heliu în cazul tratamentului pentru astm, sufocarea este prea mică, dacă luați puțin timp pentru a ușura viața bolnavului. Similar cu heliul, „xenon” povitra (80% xenon, 20% acru), atunci când este inhalat, este un drog puternic narcotic, așa că puteți cunoaște medicamentul.
Neonul și argonul sunt utilizate pe scară largă în inginerie electrică. Când a trecut strumu electric kryz zapovneni cu gaze de trabucuri au fulgerat conductele de gaz pentru a începe să se aprindă, să rămână blocate pentru înregistrarea literelor ușoare.
Tuburile de neon necesare de acest tip sunt potrivite în special pentru faruri și anexe de semnalizare, astfel încât lumina să nu fie mult ascunsă de ceață. Cantitatea de heliu ușor din lume își schimbă prinderea în țeavă, trecând de la gură prin gură la verde. Ar, Kr și Xe sunt caracterizate prin diferite tipuri de culoare blakite.
Argonul (adăugați azot din suma de 14%) poate fi folosit și pentru depozitarea lămpilor electrice. În același timp, o conductivitate termică semnificativ mai mică este mai frumos de utilizat pentru întreaga familie de kripton și xenon: lămpile electrice furnizate cu ele dau mai multă lumină, în timp ce energia este mai multă vitalitate, este mai frumos să te uiți la instalație și în cel mai sigur mod.
Editor: Kharlamova Galina Mikolaivna